El pasado miércoles 10 de marzo tuvimos la suerte de tener una tarde entretenida con el profesor de enseñanza secundaria Alejandro del Mazo. Ya tenía la suerte de haber escuchado por parte de varias personas la labor que realiza Alejandro como divulgador de experimentos, así que como era de esperar, la sesión entera implicó una gran gama de experimentos relacionados con la física, llevados a cabo por el propio Alejandro. La lástima fue que debido a los tiempos de pandemia que estamos sufriendo, estas demostraciones prácticas se mostraron a través del otro lado de la pantalla, mediante TVUSAL, por lo que me quedó ese sabor agridulce de no poder ver in situ todas estas interesantes experiencias.
La sesión de experimentos fue dividida en cuatro grandes bloques: ondas, propiedades de la luz, electroestática y electromagnetismo. Con materiales muy sencillos y convencionales, como una simple cuerda, un tubo de PVC, globos o simplemente agua, Alejandro ha dado un repaso a todo el espectro que compone la física tanto de la ESO como del bachillerato. También es digno de destacar en su labor, que tras los experimentos, explicaba con mucha claridad a través de ilustraciones muy sencillas, el marco teórico en el que se basaba cada experiencia.
No me voy a poner a describir la multitud de experimentos que nos ha mostrado, pero si voy a describir el que más me ha llamado la atención:
FLUORESCENCIA Y FOSFORESCENCIA
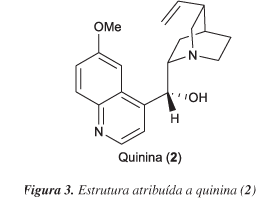
En primer lugar, el maestro Alejandro del Mazo iluminó varios recipientes que contenían diferentes sustancias. Al incidir sobre ellas un haz de luz (debe de ser UV), estas sustancias se iluminaban inmediatamente con diferentes colores, sin embargo, al dejar de incidir la fuente luminosa, las sustancias dejaban de emitir ese color, Entre estas sustancias destaca la tónica, en cuya composición presenta quinina, una sustancia fluorescente, que emite luz de color azul al ser irradiada por una fuente lumínica. Otra de las sustancias que fue sometida a la radiación UV fue la clorofila, emitiendo está radiación de color rojo intenso. Y por último fueron irradiadas sustancias como la rodamina (emite fluorescencia de color naranja) y la fluoresceína (emite fluorescencia de color amarillo-verdoso).
Todas estas sustancias que emiten fluorescencia tienen en común que en su estructura presentan anillos aromáticos y son muy rígidas. Este hecho favorece que las sustancias presenten fluorescencia, como es el caso de las estructuras de la quinina y la clorofila que aparecen debajo.
A continuación, puso otro tipo de material que, tras irradiarle con luz ultravioleta, mantenía la emisión de luz a diferencia de las sustancias anteriores. Fue el mismo caso que podemos observar en los carteles indicativos de salida de emergencia.
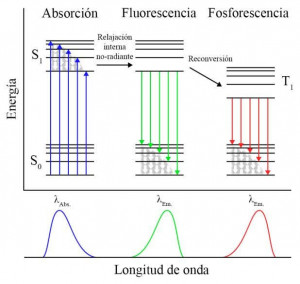
Para explicar esto, ambos procesos son fotoluminiscentes, que como su propio nombre indica, es un fenómeno que consiste en la emisión de luz inducida por fotones. Y como se apreció en la experiencia llevada a cabo por Alejandro, ambas experiencias mostraron una notable diferencia:
- Fluorescencia: la emisión tuvo lugar sólo mientras se iluminaba y, por tanto, esta cesó al desaparecer la fuente de excitación.
- Fosforescencia: la emisión se dio durante y después de iluminar debido a que existe un retraso temporal entre la absorción y la reemisión de fotones, de ahí que se observase durante un mayor periodo de tiempo este proceso.
Y por qué se observan estas diferencias. Pues muy sencillo, las transiciones electrónicas nos dan la respuesta. En las transiciones electrónicas que causan la fluorescencia no cambia el espín del electrón, lo que conlleva que los estados excitados de fluorescencia presenten una vida muy corta (alrededor de nanosegundos). En cambio, en la fosforescencia si existe un cambio en el espín del electrón, lo que repercute en que el tiempo de vida de los estados excitados sean más largos, del orden de los segundos e incluso minutos.
Para finalizar, me quedo con las siguientes reflexiones tras la sesión experimental:
- Sin ir al laboratorio, y por tanto, si no se acompañan la docencia tanto de la física como de la química con prácticas, no tienen ningún sentido estas asignaturas. Ambas como ciencias experimentales, se tienen que apoyar en las experiencias de laboratorio.
- Los alumnos por el mero hecho de observar hechos físicos y químicos, muestran una mayor curiosidad y por tanto un mayor interés en estas materias. Y si ya se los da el protagonismo y realizan ellos mismos las experiencias, aumentará más su atención.
- Con materiales muy económicos y una infraestructura muy sencilla, se pueden explicar muchos fenómenos físicos y químicos, por lo que esto no es impedimento para llevar a cabo estas experiencias como futuros docentes.
BIBLIOGRAFÍA
Maíllo, S. V., del Mazo Vivar, A., & Sánchez, M. J. S. (2019). Experimenta: 75 experimentos de física con materiales sencillos para ESO y Bachillerato. Ediciones Universidad de Salamanca.
del Mazo Vivar, A., Velasco Maíllo, S., & García Molina, R. (2017). Oír Y Ver. 61 Experimentos De Acústica Y Óptica. Editum. Ediciones de la Universidad de Murcia.
https://www.ugr.es/~decacien/Planes/Quimica/Plan%201997/temarios/671111d-archivos/fundamentos/SEMINARIO%203.PDF



![620px-Chlorophyll_a_structure.svg[1]](http://diarium.usal.es/vroblesvalero/files/2021/03/620px-Chlorophyll_a_structure.svg1_-300x157.png)


Aún no hay comentarios.